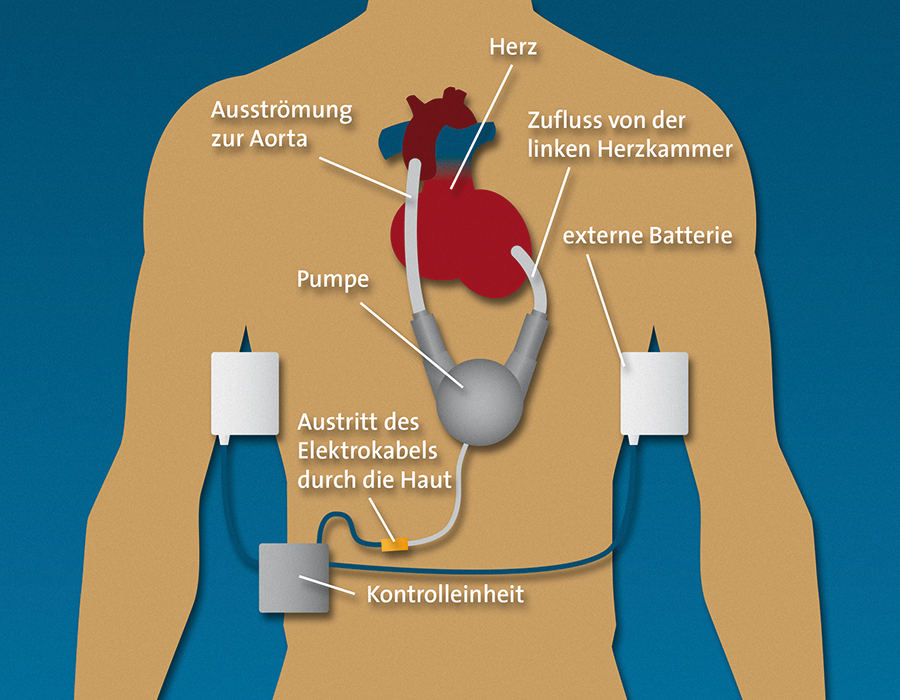
Das LVAD wird unterhalb des eigenen Herzens platziert und mit ihm verbunden. Die Stromversorgung erfolgt über ein Kabel, das an einen aufladbaren Akku angeschlossen ist.
Ein künstliches Herz – was sich im ersten Augenblick nach ferner Zukunft anhört und vielleicht auch verunsichert, ist für viele Menschen mit schweren Herzproblemen schon heute die Rettung. Das Warten auf ein geeignetes Spenderherz kann mehrere Jahre dauern – Zeit, die Betroffene oftmals nicht haben. In so einem Fall bietet die Kardiologie eine Alternative: das Kunstherz, beziehungsweise die Herzpumpe.
Das künstliche Herz ist eigentlich ein implantierbares, mechanisches Pumpsystem, welches das erkrankte Herz unterstützt. Es nennt sich „VAD“ als Abkürzung für „ventricular assist device“ oder auf Deutsch „Herzkammerunterstützungssystem“. Da das menschliche Herz zwei Herzkammern besitzt, gibt es unterschiedliche Modelle: das Rechtsherzunterstützungssystem (RVAD), Linksherz-unterstützungssystem (LVAD) und biventrikuläres Unterstützungssystem (BiVAD). Letztere werden auch totale Kunstherzen (total artificial heart, TAH) genannt. Grundsätzlich bestehen alle aus einer kleinen Pumpe und einem Elektromotor. „Welches letztendlich zum Einsatz kommt, ist individuell von der Krankheitsgeschichte des Patienten abhängig“, erläutert Kardiologe Dr. Arne Callenbach.
„Bei einer fortgeschrittenen Herzinsuffizienz, bei der mit einer schlechten Prognose zu rechnen ist, wird in der Regel die Implantation eines LVADs empfohlen.“ Dieses kann zur Überbrückung bis zur Herztransplantation eingesetzt werden. Die Pumpe unterstützt das erkrankte Herz mehrere Jahre, bis ein geeignetes Spenderherz gefunden wurde. Sollte ein Patient nicht für eine Herztransplantation infrage kommen, kann das LVAD auch als Dauerlösung implantiert werden. „Eine dritte Möglichkeit ist das Einsetzen, bis sich der Herzmuskel wieder erholt hat. Dies ist zwar selten, aber besonders bei schweren Herzmuskelentzündungen lebensrettend“, so Callenbach.
Wann braucht der Patient ein LVAD?
Grundsätzlich kommen nur Patienten mit schweren Herzmuskelschäden infrage. Die Auswurffraktion muss unter 30 Prozent liegen, das heißt: Pro Schlag wirft das Herz nur noch weniger als 30 Prozent des Blutvolumens aus, das zu Beginn der Kontraktion in der Kammer vorhanden ist. Zum Vergleich: Bei normalen Herzen liegt der Wert über 55 Prozent. Die Patienten sind somit in ihrer Leistungsfähigkeit massiv eingeschränkt. Die meisten von ihnen haben zudem bereits mehrere Krankenhausaufenthalte aufgrund massiver Flüssigkeitsansammlungen in Lunge und Beinen hinter sich. Infolge der schlechten Durchblutung der Organe kann auch ihre Nierenfunktion bereits beeinträchtigt sein.
Rückkehr zur Normalität
Im Normalfall dauert der Eingriff drei bis fünf Stunden, wobei der Herzchirurg das Kunstherz in die Bauchdecke unterhalb des Zwerchfells einsetzt. Dann wird ein Kunststoffrohr in die Spitze der linken Herzkammer gelegt und festgenäht. Über dieses Rohr wird Blut aus der linken Herzkammer in das Kunstherz transportiert. Dieses fördert das Blut dann über ein zweites Rohr in die Hauptschlagader. „Das eigentliche Herz des Patienten bleibt im Körper“, so Callenbach. Man unterscheidet pulsatile und nicht-pulsatile Herzunterstützungssysteme. Bei Ersterem wird der körpereigene Puls durch die Verwendung Druckluft- betriebener, getakteter Blutpumpen simuliert. Bei dem nicht-pulsatilen Herzunterstützungssystem wird das Blut durch kontinuierlich fördernde Axial- oder Zentrifugalpumpen gefördert. Beide Systeme sind heute die Regel. „Konsequenterweise haben die Patienten keinen fühl- oder messbaren Puls mehr“, erläutert Callenbach. Doch wie sieht es mit der Stromversorgung und Steuerung aus? „Hierzu führt ein Kabel aus dem Körper heraus, welches sich außerhalb an eine Steuereinheit anschließen lässt“, erklärt der Kardiologe. Am Tag kann die Stromversorgung durch Akkus erfolgen, die in einer Tasche am Körper Platz finden. Diese müssen allerdings alle vier bis acht Stunden aufgeladen werden. Nachts wird das Kunstherz an eine Steckdose angeschlossen. Nach der erfolgreichen Operation erholt sich der Patient zunächst ein paar Tage und muss lernen, das Kunstherz richtig zu bedienen. Dies kann bis zu ein paar Wochen dauern. „Träger eines LVADs sollten sich aber nicht entmutigen lassen“, rät Callenbach. „Es gibt weltweit Tausende von Menschen mit Herzpumpe, die wieder ein nahezu normales Leben führen.“ Sobald der Patient aus dem Krankenhaus entlassen ist, erfolgen regelmäßige Kontrolluntersuchungen. Zunächst einmal monatlich und später je nach Bedarf in größeren Abständen.
Die Risiken
Bei den Herzpumpen sind folgende Komplikationen möglich: Die Ladekabel, die von außen zur Pumpe führen, können Eintrittspforten für Infektionen sein. Zudem kann das Blut innerhalb der Pumpe verklumpen (Thrombose), weshalb alle Patienten Marcumar nehmen müssen.
Drei Arten der Anwendung
Anfänglich wurde das Kunstherz als Überbrückung bis zur Herztransplantation entwickelt, und auch heute noch ist dies die primäre Absicht. Immer mehr Patienten erhalten das Kunstherz jedoch als Ersatz zur Herztransplantation. Besonders gilt dies für diejenigen, die aufgrund ihres Alters oder Begleiterkrankungen keine guten Kandidaten für eine Herztransplantation sind. Die dritte Anwendung ist ein vorübergehender Gebrauch des Kunstherzens bei Patienten mit schweren Herzmuskelentzündungen, wobei es nach Genesung wieder entfernt wird.
Überlebenschancen mit Kunstherz
Heutige Träger eines LVADs haben eine mindestens 85-prozentige Ein-Jahres-Überlebensrate. Am 12. November 2015 erreichte der Patient Uwe S. der Medizinischen Hochschule Hannover den Meilenstein von zehn Jahren Kunstherztherapie mit dem Gerät „HeartMate II“. Er gilt als Inhaber des diesbezüglichen Europarekords als Kunstherzpatient.